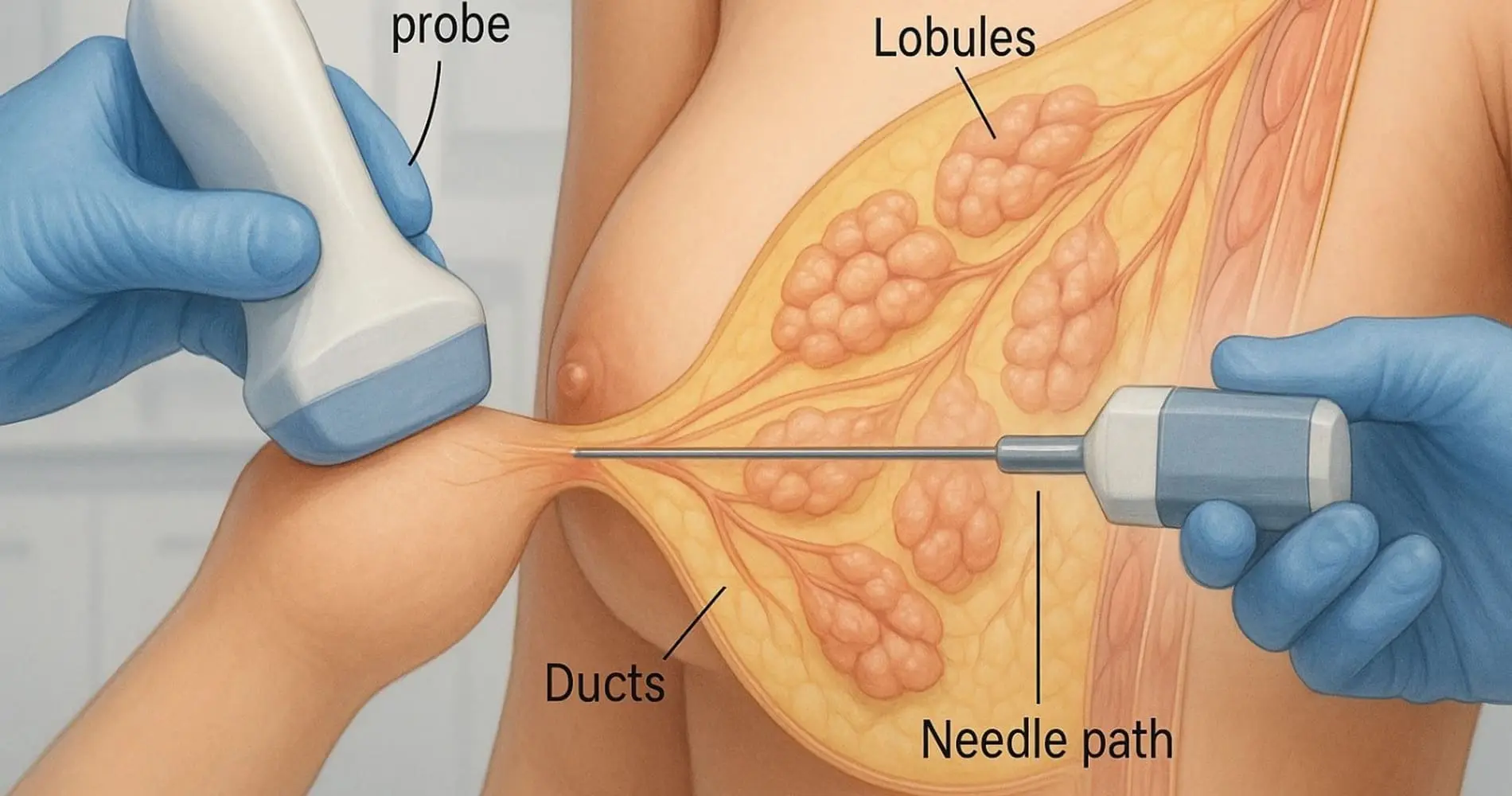
بیوپسی کبد چیست و چرا انجام می شود؟
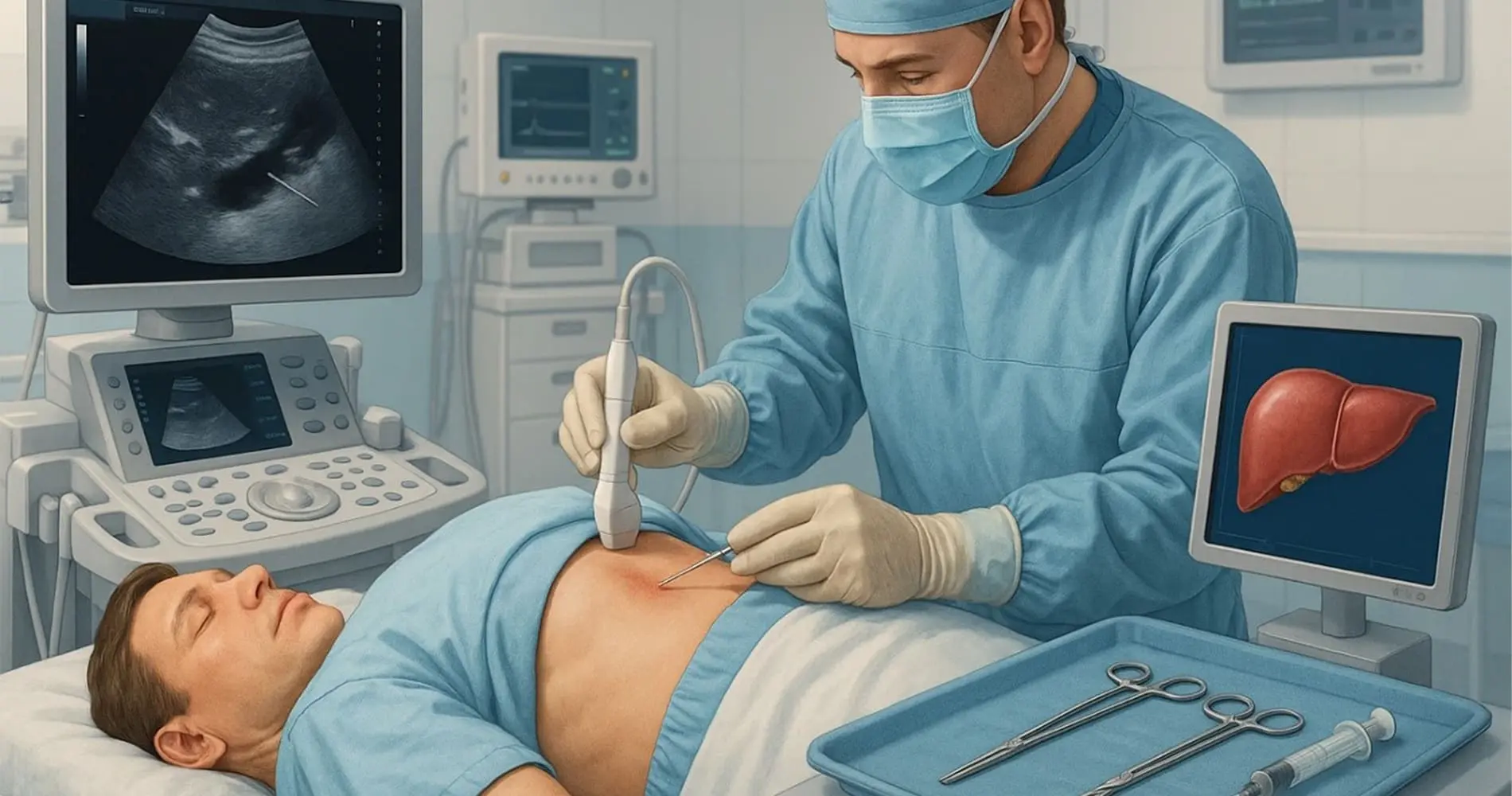
بیوپسی کبد (توده و پارانشیم) چیست و چرا انجام می شود؟
بیوپسی کبد یکی از مهم ترین روش های تهاجمی اما دقیق در تشخیص بیماری های کبدی محسوب می شود. این روش امکان بررسی مستقیم بافت کبد را فراهم میسازد تا پزشک بتواند نوع، شدت و گسترهی بیماری را بهصورت میکروسکوپی ارزیابی کند. بیوپسی کبد نه تنها در مرحلهی تشخیص، بلکه در ارزیابی پاسخ درمانی و پیش بینی پیشرفت بیماری نیز نقش کلیدی دارد.
در علم هپاتولوژی، بیوپسی به دو دستهی اصلی تقسیم میشود:
بیوپسی پارانشیمی (برای بررسی بیماریهای منتشر کبد مانند هپاتیت و استئاتوز) و بیوپسی توده ای (برای بررسی ضایعات یا تودههای مشکوک نظیر HCC و متاستازها). هریک از این دو نوع کاربرد و تکنیک خاص خود را دارند که در ادامه بررسی میکنیم.
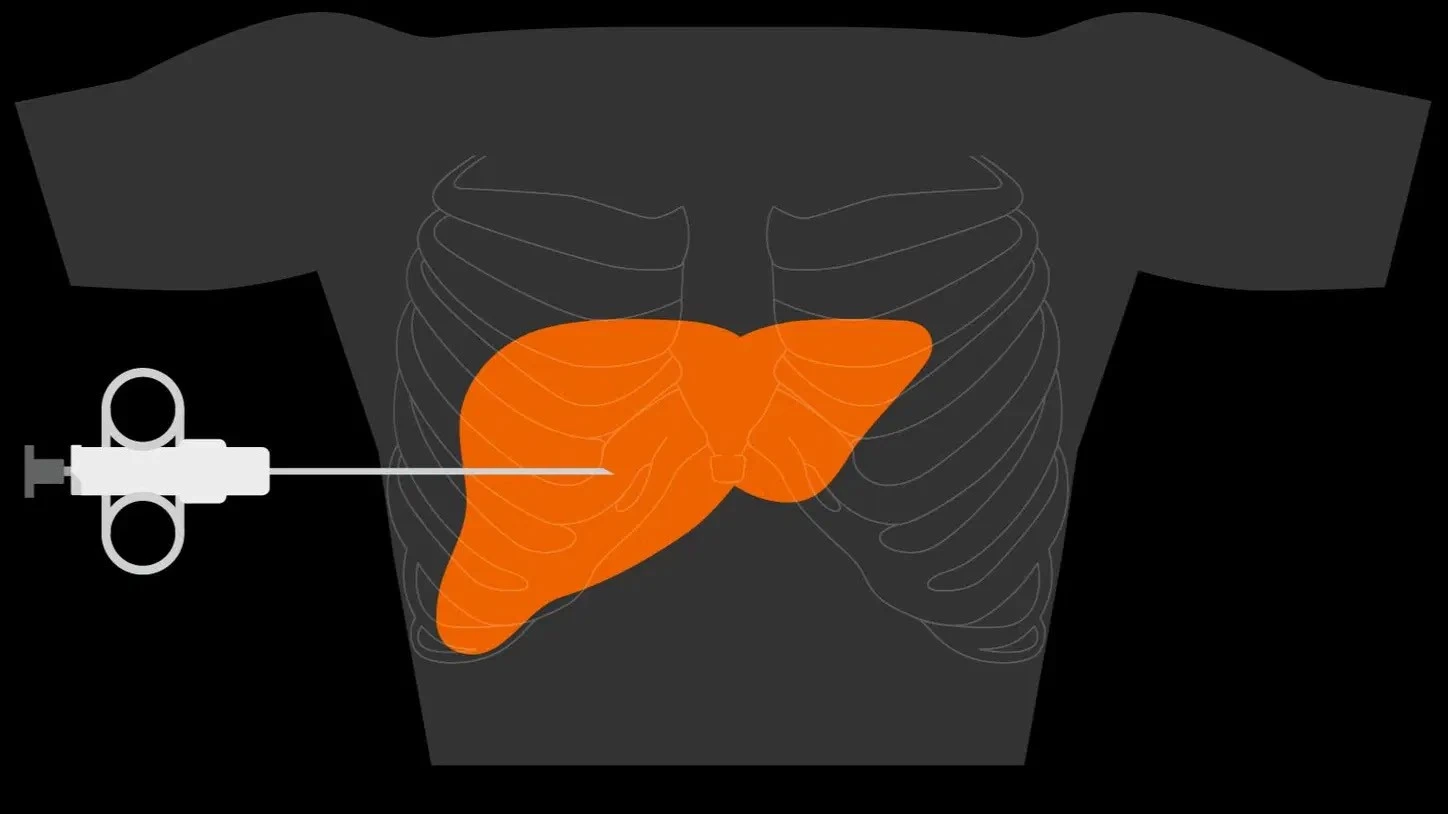
اهمیت بیوپسی در تعیین سرنوشت بالینی بیمار
تصمیمگیری در مورد درمان بیماریهای کبدی، به ویژه در مراحل اولیه کارسینوما یا تعیین شدت التهاب مزمن، نیازمند اطلاعات بافتی دقیق است. آزمایش های خون (مانند آنزیم های کبدی) و تست های تصویربرداری (مانند سونوگرافی و MRI) اطلاعات ارزشمندی درباره عملکرد کبد ارائه میدهند، اما تنها بیوپسی است که می تواند درجهی آسیب سلولی (مانند نکروز، التهاب) و میزان فیبروز (تشکیل بافت اسکار) را با دقت بالا تعیین کند.
اصول علمی بیوپسی کبد و انواع تکنیک ها
بیوپسی کبد معمولاً تحت هدایت تصویربرداری انجام میشود تا دقت و ایمنی آن بالا رود. انتخاب روش هدایت بسته به در دسترس بودن امکانات و شرایط بیمار متفاوت است. از نظر تکنیکی، بیوپسی به سه نوع اصلی تقسیم میشود که هر کدام محدودیتها و مزایای خاص خود را دارند:
- Percutaneous Liver Biopsy (بیوپسی از راه پوست):
این رایجترین روش است. سوزن بیوپسی از طریق پوست قفسه سینه یا شکم وارد پارانشیم کبد میشود. برای کاهش درد و بهبود همکاری بیمار، اغلب به صورت سرپایی تحت بی حسی موضعی و در صورت نیاز با آرامبخشی سبک انجام میشود. - Transjugular Liver Biopsy (بیوپسی ترانس ژوگولار):
این روش از طریق ورید ژوگولار داخلی گردن آغاز شده و سوزن از طریق ورید اجوف تحتانی به ورید باب کبدی هدایت میشود. این روش برای بیمارانی که اختلالات انعقادی شدید دارند یا در معرض خطر بالای خونریزی هستند (به دلیل سیروز پیشرفته یا فشار خون پورتال بالا) ارجحیت دارد، زیرا خطر خونریزی خارج کبدی بسیار پایین است. - Laparoscopic / Open Biopsy (بیوپسی لاپاروسکوپیک یا باز):
در موارد بسیار نادر، زمانی که نمونهبرداری از سایر روشها ناموفق بوده یا نیاز به بررسی همزمان سایر اندامهای شکمی وجود دارد، جراحی لاپاروسکوپیک یا لاپاراتومی باز انجام میشود.
تجهیزات نمونهگیری Core Needle Biopsy
نوع سوزن مورد استفاده معمولاً از نوع Core Needle است. این سوزنها دارای یک غلاف خارجی و یک هسته داخلی هستند که پس از نفوذ به بافت، هسته با خود استوانهای نسبتاً کامل (حدود ۱ تا ۴ سانتیمتر طول) از بافت کبد را خارج میکند. این طول برای آسیبشناس ضروری است تا بتواند ساختار کامل بافت، از جمله نمای پری سینوسی و ساختار وریدی را ارزیابی کند.
آمادهسازی بیمار پیش از بیوپسی: پروتکلهای ایمنی
آمادهسازی صحیح بیمار برای به حداقل رساندن عوارض، به ویژه خونریزی، حیاتی است. پروتکلهای استاندارد شامل موارد زیر هستند:
- ارزیابی اختلالات انعقادی
از آنجا که کبد مسئول تولید عوامل انعقادی است، اختلال در عملکرد آن اغلب با اختلالات انعقادی همراه است.
- آزمایشهای ضروری: زمان پروترومبین (PT)، نسبت نرمالشده بینالمللی (INR)، و شمارش پلاکت (Platelet Count).
- آستانه پذیرش: معمولاً INR باید کمتر از ۱.۵ و پلاکتها بالاتر از ۵۰,۰۰۰ باشد. در صورت عدم رعایت این استانداردها، نیاز به تجویز ویتامین K یا پلاکت پیش از عمل وجود دارد. - قطع داروهای ضدانعقاد
مصرف داروهایی که بر عملکرد پلاکتها یا مسیر انعقادی تأثیر میگذارند، باید قطع شوند:
- ضدانعقاد خوراکی (مانند وارفارین): قطع معمولاً ۷۲ ساعت قبل از عمل.
- ضد پلاکتها (مانند آسپرین، کلوپیدوگرل): قطع بسته به نیمهعمر دارو، معمولاً ۵ تا ۷ روز قبل. - بررسی تصویربرداری پیشارزیابی
سونوگرافی یا CT پیشارزیابی برای تعیین محل دقیق ورود سوزن ضروری است. هدف اصلی این است که مسیر سوزن از نواحی پرخطر مانند کیسه صفرا، مجاری صفراوی بزرگ، یا عروق اصلی کبد (ورید پورتال، شریان کبدی) دوری کند. - آموزش همکاری بیمار
بیحرکت بودن کامل بیمار و توانایی او در انجام مانورهای تنفسی (نگه داشتن نفس در عمق دَم یا بازدم) در لحظه نمونهگیری، برای جلوگیری از آسیب به سایر ارگانها و پارگی زودرس سوزن در بافت، حیاتی است.
روش انجام بیوپسی به تفکیک نوع و کاربرد پاتولوژیک
بیوپسی پارانشیمی (Diffuse Liver Disease Biopsy)
هدف: ارزیابی بیماریهای منتشر کبدی مانند هپاتیت ویروسی مزمن (B و C)، بیماری کبد چرب غیرالکلی (NAFLD/NASH)، هپاتیت خودایمنی (AIH)، و بیماریهای ارثی ذخیرهای (مانند هموکروماتوز).
ارزیابی پاتولوژیک: نمونهی گرفتهشده برای تعیین سه معیار اصلی بررسی میشود:
- التهاب (Inflammation): تعداد و نوع سلولهای التهابی در پارانشیم و پریپورتال.
- نکروز و آپوپتوز (Necrosis/Apoptosis): میزان تخریب سلولهای هپاتوسیتی.
- فیبروز (Fibrosis): تشکیل کلاژن و اسکار
سیستم نمرهدهی:
برای استانداردسازی شدت فیبروز، از سیستمهایی نظیر METAVIR یا Ishak استفاده میشود:
درجه METAVIR به شکل زیر است:
- F0: عدم وجود فیبروز
- F1: فیبروز پریپورتال خفیف
- F2: فیبروز با سپتومهای معدود
- F3: سپتومهای فیبروتیک گسترده
- F4: سیروز کبدی کامل
بیوپسی توده (Mass Lesion Biopsy)
هدف: تشخیص قطعی ماهیت ضایعات کانونی (تودهها). حدود ۹۰٪ از تودههای کبدی در جمعیتهای پرخطر، بدخیم هستند.
کاربردها:
- هپاتوسلولار کارسینوما (HCC):
شایعترین سرطان اولیه کبد. - متاستازها:
تومورهایی که از سایر نقاط بدن به کبد سرایت کردهاند. - آدنوم کبدی (Hepatocellular Adenoma) و FNH (Focal Nodular Hyperplasia):
ضایعات خوشخیم.
تکنیک هدایت: هدایت سوزن در این نوع بیوپسی بسیار حیاتی است و تقریباً همیشه تحت هدایت تصویربرداری (سونوگرافی یا CT) انجام میشود تا اطمینان حاصل شود که سوزن دقیقاً وارد هسته ضایعه شده و از ساختارهای حیاتی اطراف دور بماند. نمونهبرداری باید به اندازهای بزرگ باشد که آسپیراسیون سلولی (جهت سیتولوژی) نباشد، بلکه نمونه بافت (Core) باشد.
مراقبتهای پس از بیوپسی و مدیریت عوارض
دوره پس از بیوپسی دورهای است که بیشترین خطر عوارض، بهخصوص خونریزی، بیمار را تهدید میکند.
مشاهده و کنترل (Post-Procedure Monitoring)
- مدت زمان:
بیمار باید حداقل ۴ تا ۶ ساعت در بخش ریکاوری یا بستری تحت نظر باشد. - کنترل علائم حیاتی:
پایش مداوم فشار خون و ضربان قلب. - مدیریت درد:
درد خفیف تا متوسط در ربع فوقانی راست شکم شایع است و با مسکنهای غیر NSAID کنترل میشود.
عوارض جدی و علائم هشدار
اگرچه نرخ عوارض جدی بیوپسی کبد کم است (حدود ۰.۱٪ نیاز به انتقال خون)، اما شناخت علائم حیاتی است:
- خونریزی: درد شدید، تاکیکاردی (افزایش ضربان قلب)، افت فشار خون ناگهانی (شوک)، و در موارد نادر هماتوم بزرگ شکمی.
- آسیب به اندامهای مجاور: نشت صفرا (در صورت سوراخ شدن مجاری صفراوی) یا پنوموتوراکس (در صورت آسیب به ریه در بیوپسیهای فوقانی).
- عفونت: تب یا لرز پس از ۲۴ ساعت.
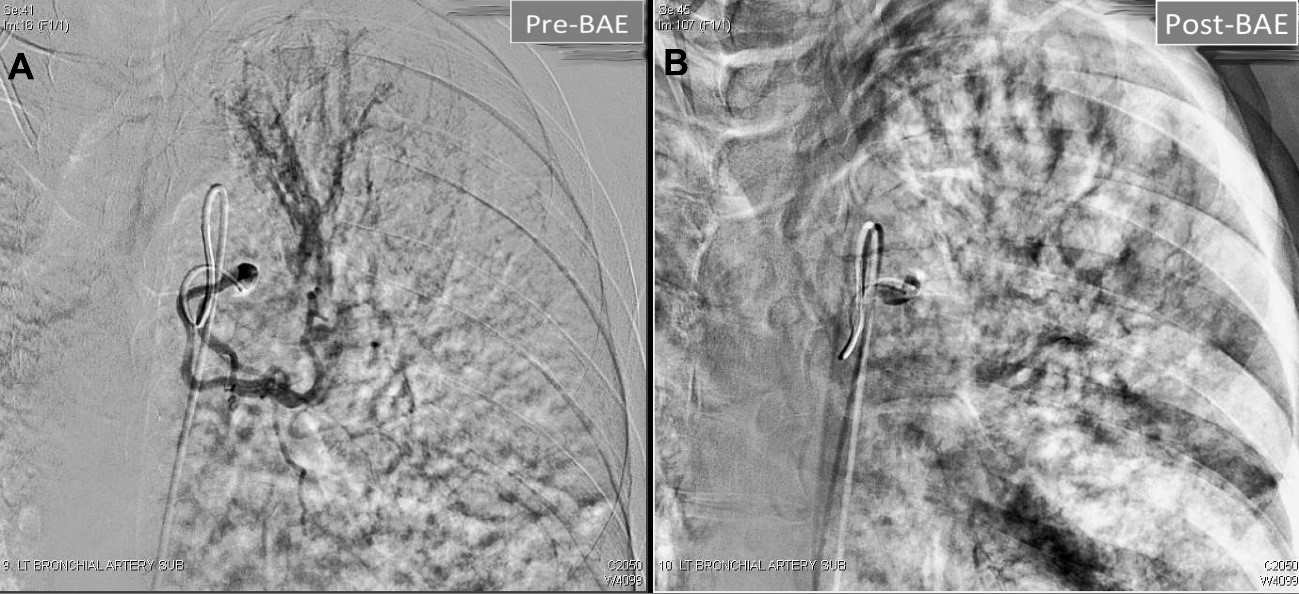
در صورت بروز علائم خونریزی شدید، اقدامات فوری شامل تزریق خون یا مایعات و در صورت لزوم، آمبولیزاسیون شریان کبدی هدایتشده با آنژیوگرافی است.
تفسیر نتایج آسیبشناسی: از ساختار تا تشخیص نهایی
آسیبشناس (پاتولوژیست) بافت نمونهبرداری شده را بر اساس چند معیار کلیدی بررسی میکند که برای تعیین استیج بیماری و پیشآگهی ضروری هستند:
رنگآمیزیهای استاندارد و تخصصی
- رنگ آمیزی پایه (H&E):
برای بررسی مورفولوژی کلی سلولها، ساختمان آچینار و حضور ذرات ذخیرهای. - رنگ آمیزی تریکروم (Trichrome):
حیاتیترین رنگ برای ارزیابی فیبروز؛ کلاژن را به رنگ آبی یا سبز نشان میدهد و امکان درجهبندی دقیق فیبروز را فراهم میکند. - رنگ آمیزی رتیکولین (Reticulin Stain):
ارزیابی شبکه کلاژنی نوع III، که در تشخیص ساختار سیروز و تومورها مهم است. - رنگ آمیزی PAS (Periodic Acid-Schiff):
برای ارزیابی ذخایر گلیکوژن و گلیکوپروتئینها. این رنگ در تشخیص برخی از نئوپلاسمها و بیماریهای ذخیره ای کاربرد دارد.
تشخیص در ضایعات تودهای
در تودهها، ایمونوهیستوشیمی (IHC) نقش کلیدی دارد.
- تشخیص HCC: مثبت شدن نشانگرهای اختصاصی مانند HepPar-1، آلفا فتوپروتئین (AFP) در بافت و گاهی اوقات نشانگرهای سیتوکریت (Arginase-1). الگوی مشاهدهشده اغلب ترابکولار یا پسودوغدهای است.
- تشخیص متاستاز: مثبت شدن سیتوککراتینهای اختصاصی منشأ تومور (مثلاً CK7/CK20 برای تومورهای رودهای).
نقش تصویربرداری در هدایت نمونهگیری: دقت و ایمنی
تصویربرداری مدرن، بیوپسی کبد و سایر بیوپسی ها را از یک روش کور به یک پروسیجر دقیق تبدیل کرده است.
روش هدایت مزایا محدودیتها کاربرد اصلی سونوگرافی (Ultrasound-Guided)در دسترس بودن بالا، هزینه پایین، عدم استفاده از اشعه یونیزان، مشاهده بلادرنگ (Real-time)محدودیت دید در کبد چرب شدید، تودههای عمیق یا خلفیبهترین انتخاب برای تودههای سطحی و بیوپسی پارانشیمی استانداردCT-Guided Biopsyدقت بسیار بالا برای تودههای عمقی، توانایی تشخیص دقیقتر بافت نرمدر معرض اشعه، زمان انجام طولانیترتودههای کوچک، عمقی، نزدیک به دیافراگم یا عروق بزرگMRI-Guided Biopsyدقت بالا در تفکیک کنتراست بین بافت نرمگران، زمانبر، عدم امکان پایش بلادرنگ دقیقضایعات با سیگنال مشابه پارانشیم (ایزودنس/ایزوواسکولار)
FibroScan (الاستوگرافی گذرا) و جایگاه آن
FibroScan یک روش کاملاً غیرتهاجمی است که از امواج الاستیک برای اندازهگیری سختی (Stiffness) کبد استفاده میکند. این روش معیاری از میزان فیبروز ارائه میدهد (مقدار اندازهگیری شده بر حسب کیلوپاسکال، kPa).
رابطه با بیوپسی:
FibroScan یک ابزار عالی برای غربالگری و پیگیری سیروز است و میتواند در بسیاری از موارد نیاز به بیوپسی پارانشیمی را کاهش دهد. با این حال، نمیتواند جایگزین بیوپسی تودهای شود و در ارزیابی دقیق التهاب، درجه نکروز یا تشخیص نوع سلولهای تومورال کاملاً ناتوان است.
آینده بیوپسی کبد و فنآوریهای نوین
علم پزشکی به سمت روشهای کمتر تهاجمی حرکت میکند، اما بیوپسی همچنان ضروری است. آینده در ترکیب دقیقتر تصویربرداری با روشهای کمکی خواهد بود:
- هوش مصنوعی در تصویربرداری (AI-Guided Biopsy):
الگوریتمهای یادگیری عمیق میتوانند تودههایی با ویژگیهای بسیار ظریف را شناسایی کرده و مسیر نمونهگیری را با دقت میلیمتری برنامهریزی کنند، که ایمنی را به شدت افزایش میدهد. - Liquid Biopsy (بیوپسی مایع):
بررسی DNA تومورال در گردش خون (ctDNA) برای مانیتورینگ پاسخ به درمان HCC. اگرچه این روش جایگزین تشخیص اولیه با بیوپسی نیست، اما برای پیگیری بسیار مفید است. - Nano-Biopsy و نمونهگیریهای با حجم بسیار کم:
توسعه سوزنهایی که نمونه بسیار کوچکتری را برداشت میکنند تا تهاجم کاهش یابد، در حالی که هنوز اطلاعات کافی برای تشخیص پاتولوژیک فراهم شود.
جمعبندی نهایی
بیوپسی کبد، چه پارانشیمی و چه تودهای، ابزاری غیرقابل جایگزین در ارزیابی دقیق و تعیین استیج بیماریهای کبدی باقی خواهد ماند. موفقیت این پروسیجر به شدت وابسته به انتخاب بیمار، مهارت رادیولوژیست مداخلهگر (با استفاده از هدایت تصویربرداری دقیق) و تفسیر دقیق آسیبشناس بستگی دارد.